Approcci terapeutici per la cura delle nefropatie
Esperienze internazionali e nazionali hanno evidenziato l’importanza di una gestione nefrologica per il rallentamento dell’evoluzione del danno renale. Sono oggi disponibili terapie farmacologiche (farmaci antipertensivi ed antiproteinurici) e provvedimenti dietologici in grado di prevenire il danno d’organo e di rallentare la progressione dell’insufficienza renale verso gli stadi più avanzati (uremia) che possono richiedere l’inizio del trattamento dialitico (emodialisi, dialisi peritoneale) o il trapianto renale.
Attualmente i farmaci che hanno dato i risultati più soddisfacenti e consolidati in termini di rallentamento della progressione del danno renale sono stati gli ace-inibitori ed i sartani; tali farmaci, conosciuti soprattutto per l’attività antiipertensiva, hanno una spiccata azione sulla emodinamica glomerulare e sulla pressione di filtrazione glomerulare oltre che sull’entità della proteinuria.
Studi più recenti hanno permesso di aggiungere a questa tipologia di farmaci gli inibitori degli SGLT2, inizialmente utilizzati nel trattamento del diabete ma che hanno evidenziato buone capacità nefroprotettive tanto da essere proposti anche nella gestione di nefropatie non diabetiche.
In campo di patologie ereditarie (es. rene policistico) vengono oggi utilizzati farmaci che hanno dimostrato la possibilità di rallentare la progressione del danno (vaptani, somatostatina).
In presenza di calcolosi renale la interazione con gli specialisti urologi permette un’ottimale gestione delle problematiche metaboliche urinarie e riduce il rischio di recidive di malattia.
Alla terapia farmacologica vanno affiancati provvedimenti dietologici da adeguare al livello funzionale (dieta ipoproteica) che risultano in grado di ridurre il carico di lavoro dei nefroni residui.In tutte le diverse fasi funzionali è importante ottimizzare i valori di pressione arteriosa e correggere anche con provvedimenti farmacologici i fattori metabolici (dislipidemia, glicemia, uricemia, obesità) che possono aumentare il rischio cardiovascolare; l’integrazione di adeguati stili di vita (cessazione abitudine tabagica, regolare attività fisica) con la terapia farmacologica risulta essenziale.
L’intervento specialistico nefrologico è essenziale nella precoce impostazione terapeutica, nel monitoraggio funzionale e nella gestione delle complicanze legate alla insufficienza renale.
Progressione e monitoraggio della malattia
Alcune malattie renali, se diagnosticate e curate precocemente, possono guarire o stabilizzarsi. In caso di cronicizzazione del danno d’organo si registra una progressione nel tempo ed una evoluzione verso la sclerosi del parenchima renale (fibrosi) associata a peggioramento funzionale (aumento della creatinina e contestuale riduzione del eGFR).L’obiettivo terapeutico è quello di rallentare la velocità di progressione della malattia attraverso provvedimenti farmacologici, dietologici ed aggiustamenti dello stile di vita al fine di evitare di raggiungere le fasi più avanzate dell’insufficienza renale che possono rendere necessari provvedimenti di trattamento sostitutivo artificiale (dialisi, trapianto).
La malattia renale cronica viene definita dal gruppo internazionale KDIGO sulla base della funzione renale e della presenza di alterazioni all’esame urina da almeno 3 mesi; vengono individuati 5 stadi ingravescenti di malattia renale cronica (MRC o ChronicKidneyDisease – CKD) classificati in base al livello di filtrazione glomerulare (eGFR) e all’entità della albuminuria. Lo stadio 3 è ulteriormente diviso in stadio 3a (VFG o GFR 59-45) e 3b (VFG o GFR 44-30La proteinuria (micro e macroalbuminuria) costituisce uno dei principali fattori di rischio di progressione del danno d’organo.
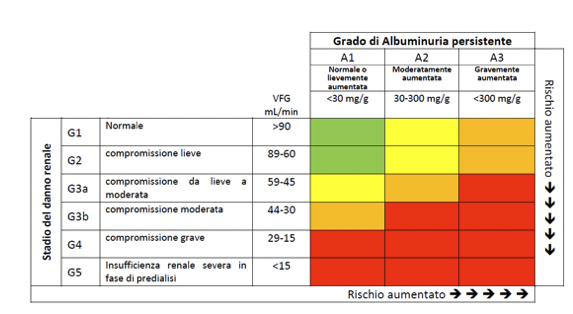
Stadi della malattia renale – da PDTA Malattia Renale Cronica Regione Emilia Romagna 2019
I pazienti con insufficienza renale presentano un rischio di sviluppare eventi cardiovascolari significativamente superiori alla popolazione generale; tale rischio aumenta con il progredire del danno funzionale e con l’entità della proteinuria.
La riduzione dei fattori di rischio correggibili è quindi essenziale nella gestione del paziente nefropatico; particolare attenzione deve essere posta al controllo della pressione arteriosa e del controllo glicemico in corso di diabete.
In caso di riscontro di alterazioni funzionali renali, soprattutto se non presenti a precedenti indagini laboratoristiche, è utile una specifica valutazione nefrologica sempre ovviamente tenendo presente la normale evoluzione fisiologica nei soggetti anziani.Il monitoraggio funzionale (creatinina, eGFR) è utile nei pazienti con nefropatia cronica; le tempistiche dei controlli, solitamente regolate nell’ambito di programmi diagnostici e terapeutici, si basano sul livello di compromissione funzionale e devono essere più frequenti in presenza di quadri più avanzati di danno renale.
Complicanze dell’insufficienza renale
La terapia farmacologica e dietologica deve tener conto del sovrapporsi delle complicanze sistemiche legate alla insufficienza renale cronica (cardiovasculopatia ed ipertensione arteriosa, anemia, osteodistrofia, alterazioni elettrolitiche, ritenzione idrosalina).
Essenziale risulta il trattamento dell’ipertensione arteriosa che costituisce un importante fattore di rischio evolutivo e possibile causa di eventi cardiovascolari.
L’impiego di diuretici risulta opportuno in presenza di ritenzione idrosalina e sovraccarico cardiocircolatorio.
Dopo valutazione del rischio di sanguinamento si possono ipotizzare anche terapie antiaggreganti.
La eritropoietina è stata essenziale nel migliorare la qualità di vita dei pazienti con moderata/severa insufficienza renale grazie alla correzione dell’anemia; stimola il midollo osseo alla produzione di globuli rossi e permette di raggiungere/mantenere target di emoglobina in grado di garantire un adeguato stile di vita e di ridurre il rischio cardiovascolare. Un ottimale utilizzo dell’eritropoietina richiede un periodico monitoraggio per evitare problemi di sottodosaggio o di ipercorrezione; l’assetto marziale deve essere periodicamente valutato ed adeguato alle esigenze dell’organismo (periodiche integrazioni).
I derivati attivi della vitamina D (in alternativa analoghi della vitamina D, calcio mimetici) sono in grado di contrastare l’iperparatiroidismo e le sue complicanze a livello osseo (osteodistrofia). I chelanti del fosforo tendono a normalizzare la fosforemia e giocano un ruolo essenziale nella prevenzione delle calcificazioni vascolari che si sviluppano nel corso dell’evoluzione del danno funzionale renale; si integrano con la gestione della vitamina D per contrastare l’osteodistrofia.
Recentemente (2022) sono entrati in commercio farmaci in grado di controllare i livelli di potassiemia soprattutto in corso di terapia con ace-inibitori o sartani; l’ottimale gestione dei valori di potassio aiuta a prevenire problematiche aritmiche.
Supplementazioni di bicarbonati contrastano l’acidosi delle fasi più avanzate di insufficienza renale.
Integrazioni farmacologiche di ferro e folina vanno personalizzate in base al quadro laboratoristico.
Tutte le diverse strategie farmacologiche si devono integrare con una corretta alimentazione, modulata sulla base del livello funzionale renale residuo. La complessità delle strategie terapeutiche richiede una gestione specialistica.
Alimentazione in corso di nefropatie
In presenza di nefropatia cronica l’alimentazione consigliata è ipoproteica (dieta ipoproteica) e normocalorica; la riduzione dell’apporto di proteine va impostata sulla base del livello di filtrazione glomerulare ed ha l’obiettivo di ridurre il carico di lavoro e di ultra filtrazione a livello delle unità funzionali renali (nefroni).Il primo provvedimento nefrologico in presenza di una alterazione funzionale renale è la limitazione dell’apporto proteico, tenendo presente che l’apporto proteico nella nostra società è solitamente superiore alle reali necessità indicate dalla Organizzazione Mondiale della Sanità. Vengono impostate diete con 0,8-0,9 gr di proteine/Kg di peso corporeo; questo apporto può essere ridotto progressivamente a 0,6 gr. Diete ancor più restrittive, utilizzate in alcuni centri nefrologici, richiedono l’integrazione di chetoanaloghi per permettere un sufficiente anabolismo proteico ed uno stretto monitoraggio nutrizionale.
In presenza di insufficienza renale la quota calorica non va ridotta se non in casi di marcato sovrappeso al fine di prevenire quadri di malnutrizione che costituiscono una situazione di pericolo e si associano ad un aumentato rischio di morbilità e di mortalità. Per permettere un adeguato apporto calorico associato ad un ridotto apporto proteico, vengono utilizzate diete con prodotti privi di proteine “aproteici”.
In tutte le diverse fasi di dieta ipoproteica risulta opportuna una collaborazione con dietologi.
In presenza di una nefropatia cronica vanno sicuramente evitate integrazioni di aminoacidi o di proteine; un eccesso di integrazione proteica o diete a lungo squilibrate in senso iperproteico non risultano fisiologiche anche in persone senza problematiche nefrologiche.
Sempre opportuna risulta la limitazione dell’apporto di sodio presente nel sale da cucina (sodio cloruro), soprattutto nei pazienti ipertesi e nei pazienti con calcolosi; viene consigliato un apporto di sale da cucina inferiore ai 5-6 grammi al giorno; la dieta ipoproteica permette inoltre di modulare il carico di potassio e di fosforo.
Nelle diverse fasi della malattia renale un’adeguata idratazione costituisce un obiettivo terapeutico primario; particolare attenzione va tuttavia posta all’apporto idrico in presenza di una ridotta capacità escretoria renale (cardiopatia, sovraccarico cardiocircolatorio, disprotidemia, sindrome nefrosica).
Gestione – Presa in carico
In presenza di patologie evolutive risulta di grande importanza un riferimento continuato per il trattamento cronico e per l’eventuale intervento terapeutico in corso di problemi intercorrenti.
L’integrazione Ospedale/Territorio nella gestione della cronicità, in linea con le indicazioni nazionali (PNRR), costituisce un obiettivo di assoluta rilevanza che deve vedere la partecipazione di tutte le risorse disponibili, pubbliche e private. In una ottimale gestione del paziente nefropatico, classico esempio di “paziente fragile”, l’integrazione fra medicina di base e supporto specialistico deve beneficiare di rapporti facilitati per la discussione di casi particolari o l’analisi dell’andamento funzionale. Possono essere utili strumenti di supporto quali la telemedicina, ma soprattutto una costante attività di formazione.
Il diverso grado di coinvolgimento dello Specialista e del Medico di Medicina Generale,solitamente regolato sulla base di Piani Diagnostici Terapeutici Assistenziali (PDTA),si basa sul livello di compromissione renale; la gestione delle fasi più avanzate di insufficienza renale (eGFR<15 ml/min) compete alla struttura pubblica di riferimento per l’impostazione di eventuali programmi di terapia sostitutiva artificiale (dialisi) o naturale (trapianto).

Vaccinazioni
Il paziente con nefropatia cronica, soprattutto nelle fasi più avanzate o in corso di terapia sostitutiva artificiale (dialisi) o naturale (trapianto), presenta un quadro di immunodepressione umorale e cellulare con aumentato rischio di infezione e di gravità degli eventuali eventi infettivi. Un programma vaccinale (antiinfluenzale, anti pneumococcica, anti zoster) è particolarmente indicato in questa popolazione di pazienti come è stato ampiamente riscontrato in corso di pandemia da SarsCoV2. L’efficacia dei programmi vaccinali è tanto maggiore quanto più conservata è la funzionalità renale.
